法规撰写是药物开发过程的重要组成部分。监管文件撰稿人必须理解科学概念以及最新的法规和指导原则,以编写符合要求的监管文件。因此,为药物项目编写所需的文件可能会耗费大量时间并容易延误。
在过去的二十年里,法规撰写实践基本停滞不前。这部分是由于该领域需要更多的标准化以及对准确性和精确度的高要求。新型生成式人工智能技术有助于提高药品法规文件的编写效率。
药物研发中法规撰写的重要性
法规撰稿人将复杂的科学信息转化为针对特定受众的简洁明了的语言。这包括监管机构、医疗保健专业人员和患者。常见的法规文件包括:
- 临床试验方案
- 研究者手册
- 临床研究报告(CSRs)
- 患者叙述
法规内容的构成
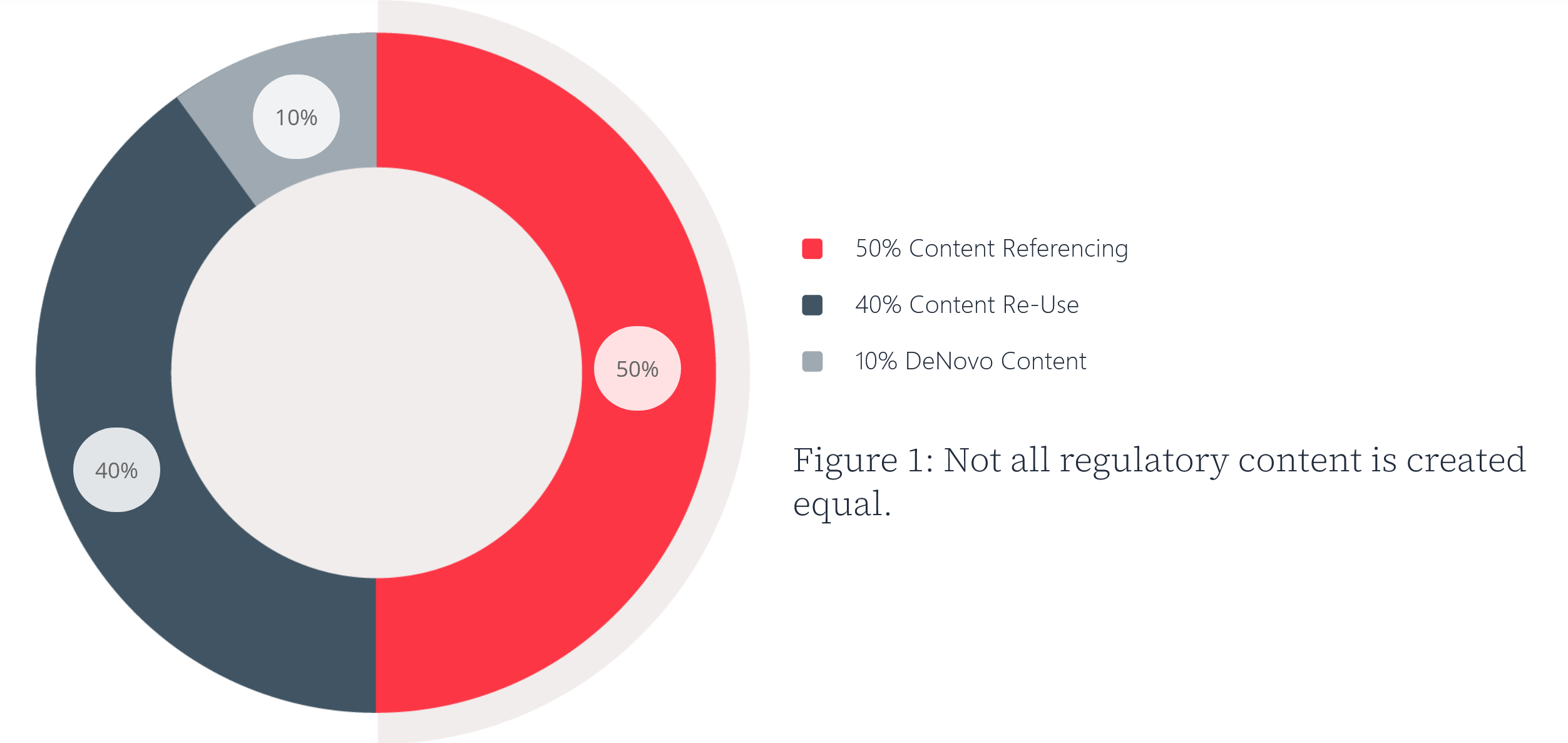
并非所有法规内容都是一样的。法规内容包括三个不同的类别:
- 内容引用: 在新内容中引用以前制作的文本、数据、表格或图像。这可以节省时间和精力,让法规撰写人在现有材料的基础上进行撰写。
- 内容复用:包括将以前编写的内容重新用于新的目的。重复使用内容有助于提高效率,同时允许撰稿人根据具体目标调整信息及其范围。
- 全新内容: 是指从零开始创建新内容。开发全新的内容可能更具挑战性,因为这需要法规撰稿人综合信息并得出结论。

50% Content Referencing
40% Content Re-Use
10% DeNovo Content
Figure 1: 并非所有法规内容都是一样的。
决定这些类别内容构成的主要因素有两个:
- 撰写标准: 一个组织的撰写标准将影响他们如何引用、重复使用或重新创建内容。
- 文件类型: 文件类型也会影响内容创建中使用的混合方法。例如,临床研究报告通常依赖于引用和重复使用。相比之下,通俗概要将更倾向于包含全新内容。
长周期时间及其原因
为了简化药物开发过程,目前正在推动缩短法规撰写的 “周期时间”。周期时间是指创建一份法规文件从开始到结束所需的时间。它包括所有相关步骤,如起草、审核、格式化和文件定稿。
尽管法规撰写人和组织尽了最大努力,但在法规撰写中,延长撰写时间的情况仍然很普遍。这是由几个因素造成的,其中包括:
- 内容的复杂性可能需要大量的研究和撰写时间
- 需要高度准确,因为即使是很小的误差也会引起监管机构的严重后果
- 全面审查和批准周期的需求可能涉及多个利益相关方
这些因素可能导致文件的编制时间大大超过最初的预期。例如,一份临床研究报告(CSR)可能需要一个法规撰写团队在四周内投入大约 120 小时(五天)的工作时间。然而,从数据库锁定到完成一份经过全面审查和批准的临床研究报告(CSR),平均需要 83 天的时间。
完成临床研究报告(CSR)的时间框架取决于团队规模、内部运营以及可用的工具和资源。
Data Finalization
Data Validation
Data Analysis
Data Delivery
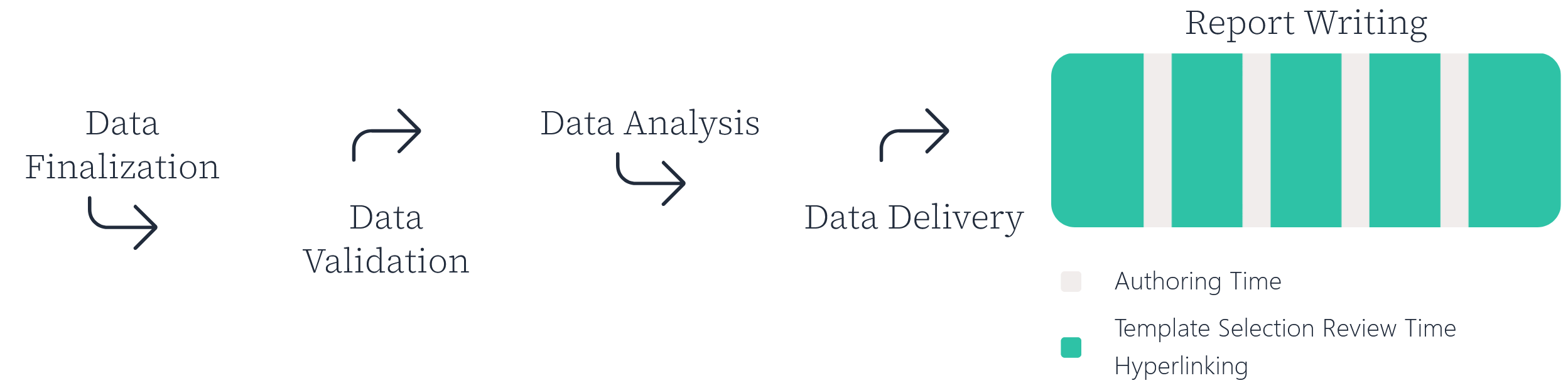
Report Writing

Authoring Time
Template Selection Review Time Hyperlinking
在法规撰写中,常常会出现长周期时间的情况。
如何加快法规文件的撰写
以下是生成式人工智能技术可以帮助法规撰稿人加快法规文件创建的一些最具影响力的方法:
- 数据集成:允许在数据库锁定前后填充数据量大的报告。这就确保了经过验证的数据在编写过程中保持完整,同时消除了人工干预。
- 使用自动化电子模板:这些工具可以通过提供框架和自动填充元素来简化写作过程。这最大限度地提高了可追溯性,节省了时间,并确保团队能够生成符合行业标准的报告。
- 复用内容: 重复使用以前编写的内容可以省时省力。这还可以减轻所需的质量审查负担。不过,确保再利用的内容仍然相关和准确至关重要。
没有放之四海而皆准的方法;每个组织可能会使用一种或几种方法。
什么是最好的法规撰写软件?
CoAuthor 是一款集成式自动法规撰写软件,采用生成式人工智能技术,可简化文档制作。CoAuthor 允许法规撰写人:
- 使用预定义模板和元数据创建一致、合规的文档,减少人工操作。
- 从各种来源和格式导入并刷新分析数据集、表格、列表和数字,确保数据的准确性和时效性。
- 与 Pinnacle 21 Enterprise 验证工具和 Certara.AI 深度学习引擎集成,以提高数据质量并生成见解。
- 与各团队和组织的多个利益相关者合作和沟通,促进审查和批准流程。
CoAuthor 使法规撰稿人能够专注于文件的关键分析、相关信息和法规要求。同时,它还能减少创建文档的时间和成本。CoAuthor 是一个全面的创新解决方案,可简化和加快法规撰写流程。
结论
医学传播是开发新药过程中耗时但至关重要的一环。确保准确性并遵守监管基准可以延长法规文件的撰写周期。然而,实施适当的策略可以让法规撰稿人加快法规文件的创建,从而简化药物开发流程。
要了解有关使用生成式人工智能自动执行重复性写作任务和利用结构化内容的更多信息,请观看我们内容丰富的网络研讨会:
参考文献
- Certara. Applying Technology to Expedite Regulatory Writing.
- Barton B, Davidson S. Good practice in medical writing. Biochem Soc Trans. 2011 Oct 1;39(5):1341–1343. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3149406/
立即预约免费演示,亲睹 CoAuthor™ 如何革新您的监管写作流程。
利用生成式 AI 加速申报时间线
通过内置 QA 工具确保合规性与一致性
依托安全可靠的机构专用 AI 技术,令您高枕无忧